Клиническое исследование
Биомеханическая стабильность зубных имплантатов в аугментированных верхнечелюстных участках: Результаты рандомизированного клинического исследования с использованием четырех различных биоматериалов и PRF, биологический взгляд на направленную регенерацию костной ткани
Авторы: Троедан Анджело,1 Вайнрайт Марсел,2 Куррек Андреас,3 и Шлихтинг Изабела4
1Институт челюстно-лицевой хирургии и стоматологии, Главная больница г. Вены «Хитцинг» , Волкесбергенстрафэ 1, павильон 3a, Вена,1130, Австрия
2Имплантологическая больница Кайзерверфа, Кайзерверфе Маркт 25, Дюссельдорф,40489, Германия
3Имплантологическая больница Оберкассел, Доминиканештрассе 10, Дюссельдорф, 40545 Германия
4Центр лицевой эстетики Вены, Браухьюсгес 12, Вена, 1050, Австрия
Корреспонденцию направлять на имя Troedhan Angelo;troed@aon.at
Научный Редактор: Девора Шварц-Арад
Все права защищены © 2015 Troedhan Angelo et al. Настоящая статья находится в открытом доступе и распространяется в соответствии с лицензией Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии, что оригинальная работа цитируется должным образом.
Вступление.
Костная регенерация происходит главным образом за счет периостальной и эндостальной гуморальной и клеточной активности, которая незначительно влияет на выбор хирургических методов и костных трансплантатов для направленной регенерации костной ткани. Данная научная работа исследует на клиническом уровне биомеханическую стабильность аугментированных участков в верхнечелюстной кости при применении нового класса формуемых, самозатвердевающих кальций-фосфатных биоматериалов (SHB), используемых с добавлением и без добавления насыщенного тромбоцитами фибрина (aPRF) методом Пьезотомически усиленного субпериостального туннеля (PeSPTT). Материал и методы. 82 пациентам с горизонтальной атрофией переднего верхнечелюстного гребня проводилось лечение PeSPTT, рандомно разделенное на двухфазное (60% HA/40% bTCP) или монофазное (100% bTCP) SHB без или с добавлением aPRF. 109 имплантатов были установлены в аугментированные участки через 8,3 месяца, и значение усилия фиксации (ITV) измерялось как клиническое выражение (био)механической стабильности аугментированной кости и сравнивалось с ITV предыдущего исследования в области синус-лифтинга. Результаты. Достоверные, почти в два раза более высокие результаты (био)механической стабильности, выраженные более высокими ITV по сравнению с нативной костью, были достигнуты с помощью используемых биоматериалов, а более постоянные результаты с добавлением aPRF. Вывод. Использование SHB самостоятельно или в сочетании с PRF, по-видимому, благоприятно влияет на достижение превосходного (био)механического стабильного восстановления альвеолярной кости.
1. Вступление
Физиология и заживление костей после механической травмы (естественные и ятрогенные макроскопические и/или микроскопические переломы) хорошо известны в общей медицине уже давно [1] и биологически определяются основной функцией периоста и эндоста [2, 3] на основании их гистологического состава[4].
Экспериментально и клинически доказано образование кости «de novo» под приподнятой мембраной Шнейдера в процедурах синус-лифтинга [5] даже при отсутствии ауто-/гетеро-/ксеногенных или синтетических биоматериалов [6], поскольку мембрана Шнейдера состоит в основном из надкостницы, выстилающей костные стенки верхнечелюстной пазухи [7] (Рис. 1)
Очевидно, известный жизненно важный факт функции периоста и эндоста как основного носителя заживления и регенерации костей долгое время, игнорировался в челюстно-лицевой хирургии и имплантологии [8], что привело к многочисленным исследованиям, посвященным гипотетической остеоиндуктивности и/или остеокондуктивности ауто-, гетерологичных и ксеногенных костных трансплантатов в сравнении с синтетическими биоматериалами [9 – 15]. Только недавно проводилось исследование, сохраняет ли применяемая хирургическая техника, например синус-лифтинг, неповрежденную и приподнятую надкостницу или просто приводит к рассечению надкостницы от респираторного эпителия [16], что приводит к неудачам в процедурах направленной костной регенерации (GBR). Напротив, доказанная чистая периостальная отслойка [7] обеспечивает более высокие и постоянные показатели успеха при синус-лифтинге [17] даже при менее активном[17] ремоделировании бокового отдела верхней челюсти [18].
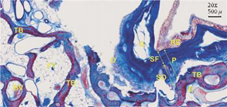
Рисунок 1: Образец среза верхнечелюстной пазухи человека после отслоения мембраны Шнейдера методом tHUCSL- INTRALIFT в голове свежего трупа человека. RE: респираторный эпителий, направленный внутрь верхнечелюстной пазухи, P: надкостница (общая), SF: подраздел надкостницы (P): фиброзный слой (stratum fibrosum), SO: подраздел надкостницы (P): остеогенный слой (stratum osteogenicum), O: остеобласты (красные точки), TB: трабекулярная кость (красноватая), E: эндост (синий слой, покрывающий всю TB), G: железа, BV: кровеносный сосуд и FT: жировая ткань. Образец при 20-кратном увеличении готовили путем иммерсионной фиксации в 5%-ном нейтрально-формальдегидном растворе, обезвоживали спиртом, закладывали в Парапласт и разрезали микротомом на кусочки по 5-6 мкм. Азан-окрашивание проводили с целью визуализации остеобластов в надкостничном слое (красноватый цвет), коллагеновых волокон надкостницы и соединительной ткани синус-мембраны, а также соединительных волокон Шарпея (темно-синий цвет).
Как с биологической, так и с физиологической точки зрения процедуры синус-лифтинга, независимо от того, выполняются ли они с латеральным или транскрипционным подходом, технически должны рассматриваться как «субпериостальный туннель» или «карманные» методы, создающие костный и закрытый субпериостальный каркас для направленной регенерации кости (GBR) без необходимости поднимать слизисто-надкостничный лоскут полной толщины, особенно в транскрестальных процедурах [17].
Метод субпериостального туннеля (SPTT) для реконструкции атрофических альвеолярных гребней в верхней и нижней челюстях был впервые описан в 1982 г. [19], а позже оценивался увеличением числа пациентов использующих непористую гидроксиапатитовую керамику (HA) [20], но при применении метода отмечалось смещение подвижных гранул в период заживления [21]. Усовершенствование методики для получения более предсказуемых результатов было представлено в 1991 году с использованием непористого HA, заблокированного в резорбируемой Викриловой трубке [22] или микропористого HA с механической стабилизацией субпериостального туннеля хирургической шиной [23]. Эти методы улучшили результаты, достигнутые с помощью SPTT в отношении увеличения вертикальной высоты атрофической нижней челюсти за счет лучшей иммобилизации синтетического костного трансплантата, и позволили улучшить стабильность съемных протезов. Были исследованы различные биоматериалы и добавление рекомбинантного человеческого тромбоцитарного фактора роста BB (rhPDGF - BB) в отношении регенерации костной ткани с помощью SPTT [24], сопоставлены с результатами, полученными с использованием тех же биоматериалов и rhPDGF-BB в процедурах синус-лифтинга [25], а также инъекционных гидрогелей на основе гиалуроновой кислоты с наногидроксиапатитом [26]. Однако, известна абсолютная потребность в правильной иммобилизации металлического имплантата в кости за пределами биологического порога для достижения полной остеоинтеграции ортопедического имплантата [27,28]. Зубные имплантаты [29],такие как SPTT, долгое время игнорировались в направленной костной регенирации (GBR), и должны применяться также к частичным костным трансплантатам, используемым для GBR в челюстно-лицевой хирургии: они следуют точно такой же схеме остеоинтеграции [30, 31], но могут позже подвергнуться резорбции и/или замене нативной костью в естественном цикле костного ремоделирования [32].
При сравнении как минимально инвазивный транскрестальный синус-лифтинг, так и субпериостальный туннельный метод обеспечивают субпериостальный каркас с костным основанием верхнечелюстной кости, который затем заполняется девитальными (свободными) аутологичными, ксеногенными или синтетическими костными трансплантатами (Рис.2) для создания достаточного объема будущей кости и биомеханически стабильной крестообразной кости для установки зубного имплантата. Биомеханические свойства восстановленного альвеолярного гребня (или субантрального увеличения) и удовлетворительный долгосрочный прогноз имплантации лучше всего выражаются более высокими значениями усилия фиксации (ITV), определяемыми при вставке зубного имплантата в увеличенный альвеолярный гребень (или субантральное увеличение) по сравнению с естественной верхнечелюстной костью [33].. Поскольку успешному восстановлению альвеолярного гребня в своевременном процессе заживления после GBR обязательно предшествует достаточный ангиогенез и васкуляризация матрицы, особенно при критических дефектах размером более 2,7 мм [34] , необходимо строго учитывать высокочувствительный к механическим воздействиям характер этого процесса [35]: макро- и микромодуляции отделения слизистой оболочки при мышечной деятельности во всей полости рта и вокруг нее, вокруг челюстных костей и внутри верхнечелюстной пазухи при дыхательной деятельности вообще не могут быть предотвращены, но могут быть облегчены усилением предшествующего ангиогенеза в цикле заживления. Это усиление предположительно приписывалось насыщенной тромбоцитами плазме (PRP) [36] или, относительно недавно, насыщенному трамбоцитами фибрину (PRF) [37, 38], его свойства усиливает остеогенная дифференцировка мезенхимальных стволовых клеток, происходящих из пери- и эндоста[39, 40].
Поэтому практикующий врач в своей повседневной рутинной работе должен полагаться на GBR-методы, биоматериалы и процедуры трансплантации, которые обеспечивают надежные и воспроизводимые результаты для возможной установки успешного долгосрочного зубного имплантата, выраженные легко получаемыми и проверенными надежными клиническими параметрами, такими как значение усилия фиксации (ITV) при установке имплантата [41-43].
Цель настоящего исследования заключается в изучении получившихся результатов биомеханической стабильности восстановленного альвеолярного гребня после завершения костной регенерации при использовании двух различных формуемых и самозатвердевающих кальций-фосфатных заменителей костного трансплантата [30] с использованием метода субпериостального туннеля в передней челюсти для определения того, сможет ли этот новый класс биоматериалов, по присущему ему физическому свойству требуемой иммобилизации [35] аугментационного каркаса, достичь последовательных результатов, выраженных сравнимыми или более высокими значениями ITV по сравнению с природными челюстно-лицевыми костями, а также воздействию насыщенного тромбоцитами фибрина (PRF) [31] при добавлении в костный блокоподобный биоматериал. Затем полученные результаты сопоставили с результатами аналогичного исследования [33] , изучающего механическое качество восстановленной субантральной кости с использованием четырех различных давно используемых и хорошо документированных биоматериалов при транскрестальном синус-лифтинге, чтобы продемонстрировать предлагаемое биологическое и клиническое сходство между этими двумя различными хирургическими методами.
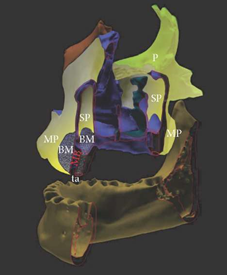
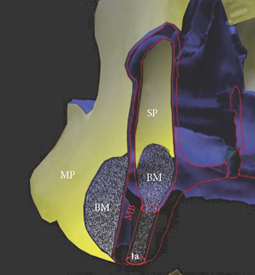
Рисунок 2: Графическое изображение корреляции анатомических и биологических сходств синус-лифтинга против буккального поднадкостничного туннеля методика-увеличения-участков (обзор (а), детали (b); периостальный покров всех костных поверхностей, изображенный желтым цветом) MB: очертания верхнечелюстной кости (красный) MP: надкостница, покрытая слизистой оболочкой полости рта, SP: синусовая надкостница верхнечелюстной пазухи, P: периостальный покров костей лицевого скелета, BM: биоматериал применяется субпериостально в синус-лифтинге и т.п.: транскрестальный подход метода tHUCSL-INTRALIFT.
2. Материал и методы
82 последовательных регулярных пациента, имеющих право на направленную регенерацию костной ткани в передней челюсти от резца до клыка с достаточной высотой альвеолярного гребня не менее 14 мм и шириной альвеолярного гребня менее 3 мм получили лечение методом Пьезотомического усиленного субпериостального туннеля (PeSPTT). Пациенты были в возрасте от 29 лет до 71 года.
У этих пациентов были аугментированы 82 субпериостальных туннельных участка от первого резца верхней челюсти до клыка, а после периода заживления было вставлено 109 имплантатов. Всем пациентам проводилась антимикробная защита либо Амоксициллином/Клавулановой кислотой по 1 г 2 раза в день, либо Клиндамицином по 300 мг 3 раза в день в течение 5 дней, начиная за один день до операции.
26 пациентов с высотой альвеолярного гребня не менее 14 мм и шириной не менее 5 мм служили контрольной группой естественной верхнечелюстной кости в переднечелюстной области, получавших те же имплантаты, что и исследуемые группы (одноступенчатый Q1-имплант, 3.5/14 мм, TRINON Karlsruhe GmbH/ Германия), в результате чего было получено 30 переднечелюстных имплантатов (n = 30).
Поскольку метод субпериостального туннелирования является научно обоснованной и документированной хирургической процедурой, а выбранные биоматериалы сертифицированы в Европейском Союзе, в соответствии с руководящими принципами EMEA для этого клинического исследования не требовалось никакого одобрения со стороны этического комитета. Каждый пациент подписывал согласие на получение сертифицированного биоматериала, выбранного случайным образом, а также, возможно, насыщенного тромбоцитами фибрина (aPRF), полученного из аутологичной крови.
Для достижения стандартизированного воспроизводимого чистого отделения интактной надкостницы от кости (Рис. 3 и 4) при создании субпериостального туннеля использовали ультразвуковое устройство (Piezotome II или Implantcenter II/Satelec-ACTEON/ France) для подготовки с помощью наконечника BS 4.
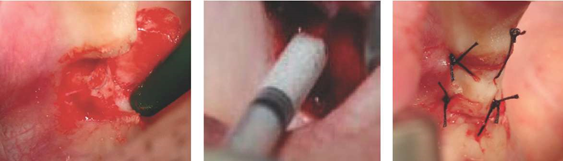
После клинического осмотра (Рис.5) был сделан вертикальный мукопериостальный разрез, приблизительно 10 мм, мезиального участка аугментации 5-8 мм (Рис. 6) с последующей подготовкой субпериостального туннеля с помощью ультразвукового рабочего наконечника BS 4 (Рис. 7(а)), прикрепленного к ручному фрагменту Пьезотома II или устройству Implant Center II (Рис. 7(b)). Затем вход в туннель проверялся на ширину (Рис. 8), чтобы обеспечить возможность введения шприца с биоматериалом (Рис.9) и при наличии дополнительного слоя aPRF-мембраны (Рис. 10(а) ). Для достижения сопоставимых и непредвзятых результатов на каждый участок зуба наносили 1 см3 биоматериала ( т. е. 1 см3 для отсутствия одиночного зуба, 2 см3 для промежутка от двух отсутствующих зубов и т. д.). После формования и затвердевания биоматериала естественным кровотоком или инъекцией aPRF-жидкости вертикальный разрез закрывали одношовными швами (Рис. 11).
Формуемый и затвердевающий на месте биоматериал, а также добавленный aPRF были распределены случайным образом (Excel Random Generator formula "=RUNDEN(ZUFALLSZAHL()*2; 0)+1") в трех спецификациях:
[1] easy-graft CRYSTAL, размер гранул 0,45-1 мм (SUN-STAR Degradable Solutions AG/Zurich/CH): микропористые составные частицы 40% бета-трикальцийфосфата (beta-TCP) и 60% гидроксиапатита (HA),где каждая частица покрыта 10-микрометровым слоем полимолочно-со-гликолевой кислоты (PLGA); первичные свободные частицы перфузируются «Биолинкером» (раствор N-метил-2-пирролидона) и после того, как Биолинкер вымывается естественным кровотоком, затвердевает до прочного участка, заменяющего костную ткань (назначенные места имплантации: n = 36);
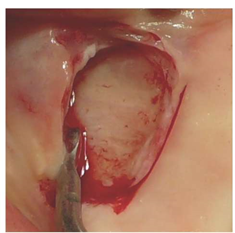
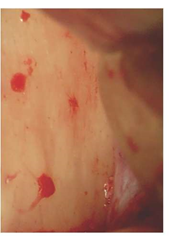
Рисунок 3: Макроскопическая клиническая демонстрация чистой отслойки надкостницы от кости с помощью Пьезотомической хирургии с использованием кавитационного эффекта: на кости не видно остатков остеогенного слоя надкостницы; перфорирующие кровеносные сосуды чисто разрезаны.
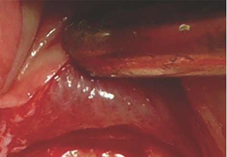
Рисунок 4: Крупным планом вид ревертированной надкостницы, чисто отделенной от кости с помощью Пьезотомической операции во время подготовки к процедуре субпериостального туннеля. Интрапериостальная сосудистая сеть видна и неповреждена.
(2) easy-graft CLASSIC, размер гранул 0,5-1 мм (SUN-STAR Degradable Solutions AG/Zurich/CH): микропористые частицы химически чистого бета-трикальцийфосфата (beta-TCP), каждая частица покрыта 10-микрометровым слоем полимолочно-со-гликолевой кислоты (PLGA); первичные рыхлые частицы перфузируются «Биолинкером» (раствор N-метил-2-пирролидона), и как только Биолинкер вымывается естественным кровотоком, биоматериал затвердевает до прочного участка, заменяющего костную ткань (назначенные места имплантации: n = 35);
(3) easy-graft CLASSIC, размер гранул 0,5-1 мм (SUN-STAR Degradable Solutions AG/Zurich/CH): микропористые составные частицы 10% бета-трикальцийфосфата (beta-TCP) и 2% гидроксиапатита (HA), где каждая частица покрыта 10-микрометровым слоем полимолочно-со-гликолевой кислоты (PLGA); первичные свободные частицы перфузируются «Биолинкером» (раствор N-метил-2-пирролидона). Вместо того чтобы вымыть Биолинкер естественным потоком крови, Биолинкер был принудительно промыт полученной жидкостью при подготовке насыщенного тромбоцитами фибрина мембраны (aPRF/SYFAC/France) в стерильном шприце для затвердевания биоматериала и слоя aPRF помещали субпериостальный слой (назначали места имплантации: n = 38).
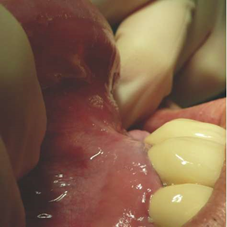
Рисунок 5: Предоперационное клиническое обследование латерального атрофического альвеолярного отростка.
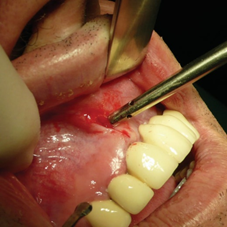
Рисунок 6: Вертикальный разрез мезиального участка аугментации (левый1- й и2- й резцы).
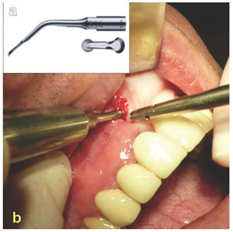
Рис. 7: (а) рабочий наконечник BS-4 для Пьезотома II/SOLO/Implant Center II. (b) чистая отслойка надкостницы от верхнечелюстной кости с помощью Пьезотом-устройства до базальных краев носовой полости.
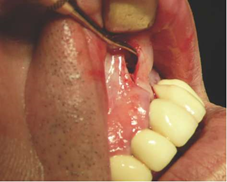
Рисунок 8: Осмотр субпериостального туннеля и зондовое тестирование на наличие достаточных карманных расширений в области левого клыка.
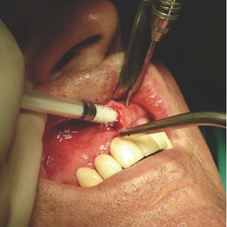
Рисунок 9: Введение формуемого и затвердевающего на месте биоматериала.
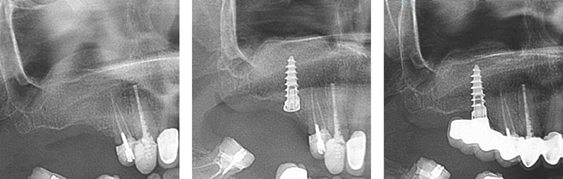
Через 6-7 месяцев была проведена контрольная CBCT участка аугментации для проверки размеров кости для планируемого введения имплантата (Рис. 12).На заре возникновения современной эндодонтии существовало множество концепций, стратегий и техник для препарирования корневых каналов. За последние десятилетия появлялись десятки инструментов для прохожде-ния и формирования каналов.


(a) (b)
Рис. 10: а)подготовка PRF для нанесения на чистый биоматериал с твердеющим bTCP «in situ» при рандомном разделении. PRF-сгустки будут сжаты, чтобы сформировать эластичную мембрану, а выделенная жидкость аспирирована стерильным шприцем для последующего вымывания Биолинкера, чтобы биоматерил затвердел до импланта, заменяющего костную ткань. С помощью этой процедуры активные ангиогенные и остеобластстимулирующие клетки перфузируются внутри затвердевшего пористого участка биоматериала. (b)измерение крутящего момента с шагом 1 Нсм с помощью Implantcenter II, импланта мотора.
По результатам исследования, изучающего среднее время завершения регенерации костной ткани в процедурах синус-лифтинга [6] и для достижения объективного сравнения с результатами, полученными в исследовании синус-лифтинга [33], имплантаты были вставлены после среднего времени заживления 8.3 месяца (максимум: 8.6 месяца, минимум: 7.9 месяца).
Во всех случаях один, два или три одноступенчатых Q1-имплантата (самоконусные, корневые аналоговые винтовые конструкции; TRINON-Karlsruhe GmbH / ГЕР.) с равномерными размерами 14 мм длиной и диаметром 3,5 мм вставлялись в место аугментации после верхнего крестообразного разреза и минимальной реверсии слизисто-надкостничных лоскутов на буккальную и небную стороны для клинического осмотра альвеолярного гребня (Рис.13,14(a), и 14(b)). Для достижения объективных результатов Q1-имплантаты (Рисунок 14(a)) были вставлены другим хирургом, а не хирургом, выполняющим процедуру субпериостального туннеля и случайным образом назначающим биоматериал.
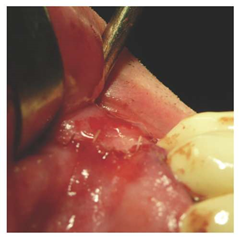
Рисунок 11: Закрытие раны одиночными стежками.
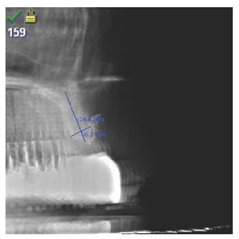
Рисунок 12: CBCT контроль и измерение достигнутых размеров костей до установки имплантата.
Определение значение усилия фиксации (ITV) было сделано с использованием Implantcenter II (Satelec-ACTEON/FR) на каждом установленном импланте, что позволило увеличить крутящий момент на 1 Нсм до 100 Нсм (Рис. 10(Б)). Установка имплантата начиналась с базовой установки крутящего момента в 15 Нсм, увеличивающейся с шагом 1 Нсм до тех пор, пока одноступенчатый Q1-имплантат не был вставлен на полную длину 14 мм. Все имплантаты шли с временными, анатомически правильными композитными коронками без окклюзионных контактов в течение 3 месяцев.
Статистическая оценка проводилась проводилась с помощью одностороннего ANOVA-теста, параметрического t-критерия Стьюдента, и по полученным результатам множественных сравнений по наименьшей значимой разнице критерия Фишера (LSD) для проверки средних значений момента вставки и дисперсии в каждой группе и средней значимости различий между всеми группами. Кроме того, данные были изображены в виде зубчатых коробочных графиков, чтобы показать распределение данных и межквартильные размахи (IQR) между 25-м и 75-м процентилями конкретного тестируемого биоматериала.
Затем результаты были сопоставлены с результатами предыдущего аналогичного исследования на дрель-крутящий момент и значение усилия фиксации после синус-лифтинга методом tHUCSL-INTRALIFT с использованием четырех различных биоматериалов (Bio-Oss, NanoBone, easy-graft CLASSIC, easy-graft CRYSTAL)) [33]. Основные установки и периоды заживления для этого исследования были одинаковы и сравнимы с настоящим исследованием. Несколько иной размер двухступенчатого Q2-имплантата, использованного в предыдущем исследовании, математически компенсируется большей длиной одноступенчатого Q1-имплантата на 2 мм (Рис. 15).
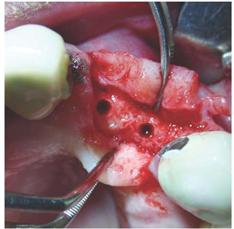
Рисунок 13: Крестообразное вскрытие участка аугментации, клинический осмотр, а также пилотное и формовочное сверление для установки имплантатов.
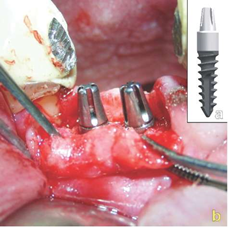
Рисунок 14: (a) Q1-форма имплантата. (b)Q1-имплантаты диаметром 3,5 мм и длиной 14 мм, вставленные в место аугментации.
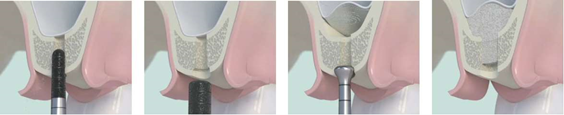
(а) (b) (c) (d)
(e) (f) (g)
(h) (i) (j)
Рисунок 15: Обзор метода tHUCSL- INTRALIFT с Пьезотом II/ SOLO:( а) дно синуса вскрывается транскрестально после возвращения минимально инвазивного крестообразного лоскута с помощью покрытого алмазом Пьезотом-наконечника TKW2, (b) герметизация сосуда подготовлена алмазным покрытием Пьезотом-наконечника TKW4, ( с) Пьезотом-наконечник TKW5 плотно вставляется в сосуд для предотвращения обратного потока жидкости в ротовую полость и субантральной потери гидродинамического давления. Затем Пьезотом активируется, и надкостница шнейдеровской мембраны чисто отделяется от костного антрального дна, используя кавитационный эффект.( d) Введение биоматериала 2 см3 в субпериостальный каркас, (e) клинический случай типичной процедуры tHUCSL-INTRALIFT, (f) субантральное применение биоматериала 2 см3, (g) закрытие раны, (h) послеоперационный рентгенологический контроль места синус-лифтинга, (i) установка имплантата в среднем через 8,7 месяца и (j) окончательное протезирование.
3. Результаты
Все операции протекали без осложнений, таких как инфекции или расхождение швов. Пациенты отмечали лишь незначительные припухлости в течение первых 5 дней послеоперационного периода и почти полное отсутствие боли (среднее значение приема ибупрофена 400 мг: 3,2 таблетки, макс.: 6 таблеток, мин.: 3,2 таблетки, макс.: 0 таблеток).Основная жалоба пациентов относилась к «ощущению объема» под губой и под носом в области аугментации, особенно когда не было прикреплено промежуточной перемычки как существовавшей ранее или недавно изготовленной временной реставрации, а только съемные частичные овердентуры без какого-либо буквального композитного щита.
Все участки субпериостального туннельного аугментирования представляли собой достаточный ровный прирост щечной кости при рентгенологическом наблюдении до установки имплантата с минимальной шириной верхнего гребня 6 мм.
Значения усилия фиксации (ITV) были самыми низкими в контрольной группе, когда имплантаты были вставлены в нативную переднюю челюстную кость (среднее значение: 27.87 Нсм, стандартное отклонение: 6,66 Нсм) (Рис. 16), но значительно (Р < 0,05) выше по сравнению с нативной верхнечелюстной костью в премолярной и молярной областях (среднее значение: 22.11 Нсм, стандартное отклонение: 4.64 Нсм) [33] (Рис. 17).
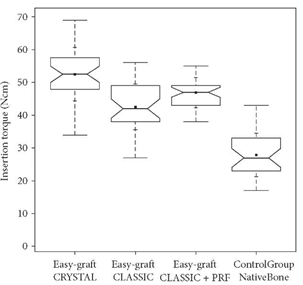
Рисунок 16: Сравнительный зубчатый график значения усилия фиксации (ITV) субпериостального туннеля в передней верхней челюсти показывает межквартильный размах (IQR) между 25-м и 75-м процентилями конкретного испытуемого биоматериала, где было расположено 50% точек данных. Кроме того, верхние усы представляют собой данные в пределах 75-го процентиля +1,5 раза выше IQR. Нижний ус разграничивает данные 25-го процентиля-в 1,5 раза больше IQR. Внутри рамок выемки обозначают доверительный интервал, основанный на медиане ± 1,58 (IQR/sqrt n) (n=количество измерений). Кроме того, среднее значение обозначается черным квадратом, а символ креста (+) отображает стандартное отклонение. Easy-graft CRYSTAL (n ==36), easy-graft CLASSIC (n ==35), easy-graft CLASSIC + насыщенный тромбоцитами фибрин (n ==38) и контрольная группа нативная передняя челюстная кость (n =30).
ITV обладали статистической (Р < 0,05) разницей между всеми группами и были наиболее высокими (среднее значение: 52.5 Нсм, стандартное отклонение: 8.15 Нсм) в группе, обработанной двухфазным самотвердеющим биоматериалом (BiSHB: 60% HA, 40% bTCP) с последующимв группе, обработанной монофазным самозатвердевающим биоматериалом (MoSHB: 100% bTCP) с добавлением насыщенного тромбоцитами фибрина (aPRF) (среднее значение 46.89 Нсм, стандартное отклонение: 4.57 Нсм) и без добавления aPRF (среднее значение: 42.51 Нсм, стандартное отклонение: 7.03 Нсм) и контрольная группа нативной кости (среднее значение: 27.87 Нсм, стандартное отклонение: 6.66 НСМ) (Таблица 1 и Рис. 16).
При сравнении ITV для BiSHB, полученных с помощью пьезо- томографически усиленного субпериостального туннельного метода (PeSPTT) в передней челюсти, с результатами исследования tHUCSL-INTRALIFT [33] средние значения ITV в группе INTRALIFT были существенно (Р < 0,05) выше (группа INTRALIFT : среднее значение: 56.58 Нсм, стандартное отклонение: 3.36 Нсм, PeSPTT группа: среднее значение: 52.5 Нсм, стандартное отклонение: 8.15 Нсм) а стандартное отклонение достоверно (Р < 0,05) ниже (INTRALIFT группа: станд. откл.: 3.36 Нсм против группы PeSPTT: станд. откл.: 8.15 НСМ) (Таблица 2 и Рис. 18).
Напротив, ITV для MoSHB с добавлением aPRF были выше при использовании для улучшенной Пьезотомом субпериостеальной туннельной процедуры в передней челюсти (среднее значение: 46.89 Нсм) по сравнению с значение: 52.5 Нсм, стандартное отклонение: 8.15 Нсм) в группе, обработанной двухфазным самотвердеющим биоматериалом (BiSHB: 60% HA, 40% bTCP) с последующимв группе, обработанной монофазным самозатвердевающим биоматериалом MoSHB без aPRF, примененным к участкам INTRALIFT (среднее значение: 45,85 НСМ), но не значимо (Р = 0,41), а также для стандартного отклонения ( PeSPTT ).: 4.57 Нсм против INTRALIFT-участков: 5.01 НСМ) (Таблица 2 и Рис. 18).
В целом стандартное отклонение как для BiSHB, так и для MoSHB без aPRF в PeSPTT-участках (SP) было значительно выше, чем в участках INTRALIFT (IL) и субпериостальных туннельных участках (SPPRF), обработанных MoSHB с aPRF (SP-BiSHB: 8.16 Нсм и SP-MoSHB: 7.03 Нсм по сравнению IL: 3.6 Нсм, IL-MoSHB: 5.01 Нсм и SPPRF-MoSHB: 4.57 Нсм) (Рис. 18).
Общее кумулятивное сравнение тестируемых сыпучих гранулярных биоматериалов (бычья кость: BioOss, синтетический трансплантат: Nanobone 100% HA, встроенный в SiO 2-матрицу) для процедуры INTRALIFT и MoSHB и BiSHB, применяемых как в процедурах INTRALIFT, так и в процедурах PeSPTT (Таблица 2), изображен на рисунке 19. Статистически значимых различий не было обнаружено при сравнении ITV контрольной группы в передней челюсти с участками INTRALIFT, дополненными бычьей костью (Р = 0,2), и MoSHB + aPRF в участках PeSPTT с участками INTRALIFT, дополненнымиMoSHB без aPRF (Р = 0,4).
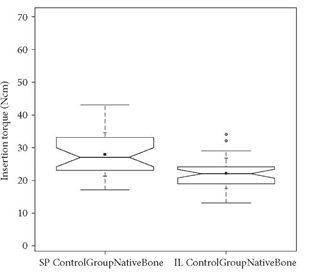
Рисунок 17: Сравнительный зубчатый график значения усилия фиксации нативной передней верхнечелюстной кости (контрольная группа субпериостальной туннельной процедуры— SP Контрольная группа Нативная кость) и нативной молярной верхнечелюстной кости (контрольная группа INTRALIFT—IL Контрольная группа Нативная кость) показывает межквартильный размах (IQR) между 25-м и 75-м процентилями исследуемого специфического биоматериала, где было расположено 50% данных. Кроме того, верхние усы представляют собой данные в пределах 75-го процентиля +1,5 раза выше IQR. Нижний ус разграничивает данные 25-го процентиля-в 1,5 раза больше IQR. Внутри рамок выемки обозначают доверительный интервал, основанный на медиане ± 1,58 (IQR/sqrt n) (n=количество измерений). Кроме того, среднее значение обозначается черным квадратом, а символ креста (+) отображает стандартное отклонение. Контрольная группа нативной передней верхнечелюстной кости SP (n = 30), контрольная группа нативной молярной верхнечелюстной кости IL (n = 35).
4. Обсуждение
Физиологический цикл костного ремоделирования является непрерывным событием и регулируется пери- и эндостом [44]. Костная масса и механическая прочность повышаются, когда нужно постоянно выдерживать увеличивающиеся нагрузки, или уменьшаются вплоть до атрофии из-за отсутствия физиологической нагрузки, как это происходит при беззубом альвеолярном гребне или общих или специфических заболеваниях костей [32]. Мышцы, сухожилия, зубы, надкостница и эндост тесно связаны и закреплены в кальцифицированной структуре кости богатыми эластином коллагеновыми волокнами Шарпи, которые «интегрируются в
Шарпеево волокно - эндост (PSE) конструктивно позволяет мускулатуре воздействовать на кость как рычаг для движения, выдерживающий статические и динамические нагрузки. Тот же принцип применим и для насыщенных эластином волокон Шарпея периодонтальной связки, которая оплетает весь альвеолярный гребень [45]. Поддержание альвеолярных гребней является результатом функциональной нагрузки зубов в пределах их «биологической ширины», а не ее предпосылкой.Богатые эластином волокна Шарпея также наиболее пригодны для распределения и ослабления напряжения на кальцифицированных структурах кости. Этот «надкостничный Шарпеев волокнисто-эндостальный континуум» вместе со связанными «действующими» органами (мышцами, сухожилиями и зубами) демонстрирует эффективную слаженную структуру относительно приложенных усилий. Таким образом, волокна Шарпея предлагаются в качестве основного пери- и эндостального триггера для увеличения костной массы и биомеханической стабильности при непрерывных повышенных нагрузках путем стимуляции остеобластов, происходящих из камбиевого слоя пери- и эндоста [45]. Напротив, отсутствие усилий представленных в кости PSE - структурным континуумом (как реакция на отсутствие физической активности или, в крайности, например, во время космических полетов при отсутствии силы тяжести) приводит к дезорганизации волокон Шарпея с последующим снижением кальцифицированной костной массы, вплоть до атрофии [46, 47], доказывающих жизненно важную роль пери- и эндоста в техническом обслуживании, ремонте и регенерации кости. Хроническая перегрузка, превышающая «ширину биологического биомеханического сопротивления», приводит к резорбции кости и возможной потере остеоинтегрированных (зубных) имплантатов, но также используется терапевтически в ортодонтии. По сравнению с длинными костями нижняя челюсть содержит большее количество коллагена и по своим структурным особенностям «вероятно, придает большую гибкость кости и делает ее более пригодной для постоянных нагрузок», ремоделирования и более высокой несущей нагрузки [48] , что может быть поддерживающим для процедур GBR в CMF и челюстно-лицевой хирургии.
Но также между челюстными костями, верхней челюстью и нижней челюстью можно обнаружить значительные различия: нижнечелюстной альвеолярный гребень обеспечивает в 2,8 раза больший объем кости по сравнению с верхнечелюстным альвеолярным гребнем и демонстрирует значительную и, в отношении переднего и заднего отделов, равномерно более высокую скорость костеобразования по сравнению с верхней челюстью, тогда как в верхнечелюстном альвеолярном гребне значительные различия костеобразования можно обнаружить в переднем отделе по сравнению с задним верхнечелюстным гребнем [18]. Эти опытные результаты, полученные в эксперименте на животных, теперь могут быть подтверждены клинически у людей, когда ITV естественной субантральной кости сравниваются с ITV в передней челюсти (Рис. 17).
В то время как PSE структурный континуум, в основном, поддерживает крестальную кость и способствует регенерации костной ткани, хирургические методы GBR, в основном создающие «дефекты критического размера» неизмеримо выше биологического порога [33], требуют подходящую иммобилизацию за пределами биологического порога [29] для аугментированной матрицы, в целом, чтобы запустить первый шаг восстановления костной ткани: правильная васкуляризация [35] и остеоинтеграция биоматериалов [[30] и/или имплантатов. Эта обязательная иммобилизация аугментационного каркаса для предотвращения инкапсуляции фиброзной ткани имплантированных трансплантатов [27-29] может быть получена традиционными хирургическими методами: свободные костные блок-трансплантаты, собранные с подбородка или латерального ветвления нижней челюсти, жестко фиксирующиеся к месту аугментации винтами остеосинтеза. Эти процедуры требуют подготовки обширных полнослойных слизисто-надкостничных лоскутов и тем самым частичного разрушения надкостницы и ее васкуляризации путем надкостничного прорезания для достижения безнапорного закрытия раны. Васкуляризация участка угментации сильно затруднена хирургическим вмешательством сама процедура. Обычно известно, что эти процедуры сопровождаются высоким риском множественных осложнений, таких как объемный послеоперационный отек (который сам по себе уменьшает кровообращение в месте операции), полная или частичная резорбция трансплантата из-за отсутствия васкуляризации, расслоение раны и осложнения донорского участка.
Напротив, результаты настоящего и аналогичных предшествующих исследований [31, 33, 37-39] предполагают минимально инвазивные хирургические процедуры, такие как tHUCSL-INTRALIFT [7] или субпериостальный туннельный метод (SPTT) для сохранения функциональной целостности надкостницы [6, 7, 33] (Рис.1 и 3).
Очевидно, что использование ксеногенных бычьих, синтетических HA и нового класса формуемых и самозатвердевающих костных трансплантатов (монофазных bTCP {MoSHB} или двухфазных HA/bTCP {BiSHB}) в процедурах направленной регенерации костей значительно повышает (био)механическую стабильность восстановленного переднего и субантрального альвеолярного гребня верхней челюсти (Рис. 19), но в два раза увеличивается при использовании BiSHBВ отличие от нативной субантральной верхнечелюстной кости по сравнению с передним альвеолярным гребнем, результирующая (био)механическая стабильность после аугментации BiSHB (60% HA/40% bTCP) и MoSHB (100% bTCP), выраженная более высокими ITV, оказывается значительно выше при значительном меньшем отклонении в участках tHUCSL-INTRALIFT по сравнению с субпериостальными туннельными аугментами в передней верхней челюсти (Рис.18). Имея такое же верхнечелюстное костное основание и сопоставимый геометрический субпериостальный каркас, содержащий сопоставимые объемы BiSHB или MoSHB (Рис. 2), ITV в передней челюсти должны быть по меньшей мере равны участкам tHUCSL-INTRALIFT, если не выше, из-за естественной более высокой костной перестройки в передней челюсти. [18].
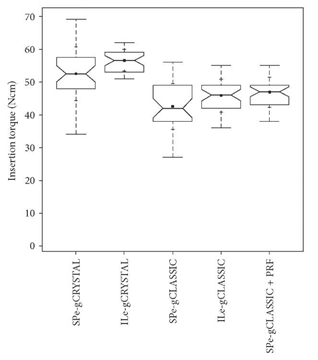
Рисунок 18: Сравнительный график значения усилия фиксации (ITV) субпериостального туннеля (SP) в передней верхней челюсти и метод iNTRALIFT (IL) с BiSHB (e-gCRYSTAL), MoSHB (e-gCLASSIC), и MoSHB + насыщенный тромбоцитами фибрин (PRF) (e-gCLASSIC + PRF) показывает межквартильный размах (IQR) между 25-м и 75-м процентилями конкретного испытуемого биоматериала, где было расположено 50% точек данных. Кроме того, верхние усы представляют собой данные в пределах 75-го процентиля +1,5 раза выше IQR. Нижний ус разграничивает данные 25-го процентиля-в 1,5 раза больше IQR. Внутри рамок выемки обозначают доверительный интервал, основанный на медиане ± 1,58 (IQR/sqrt n) (n =количество измерений). Кроме того, среднее значение обозначается черным квадратом, а символ креста (+) отображает стандартное отклонение. SPe-gCRYSTAL (n = 36), ILe-gCRYSTAL (n = 38), SPe-gCLASSIC (n = 35), ILe-gCLASSIC (n = 41), и SPe-grCLASSIC + PRF (n = 38).
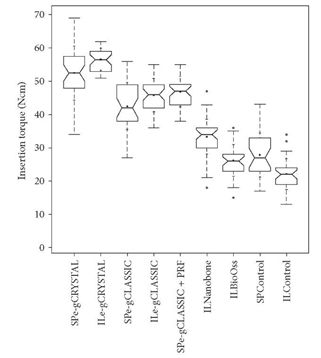
Рисунок 19: Совокупный сравнительный зубчатый график значения усилия фиксации (ITV) методом субпериостального туннеля (SP) в переднем отделе верхней и INTRALIFT- процедуры (IL) с BiSHB (e-gCRYSTAL), MoSHB (e-gCLASSIC), MoSHB + насыщенный тромбоцитами фибрин (PRF) ( е- gCLASSIC+ PRF), синтетический гранулят HA/SiO2 (ILNanobone), бычий транспарант (ILBioOss), контрольная группа SP (SPControl), и контрольной группы IL (ILControl) отображает межквартильный размах (IQR) между 25-й и 75-й процентилями конкретного испытуемого биоматериала, где расположены 50% точек данных. Кроме того, верхние усы представляют собой данные в пределах 75-го процентиля +1,5 раза выше IQR. Нижний ус разграничивает данные 25-го процентиля в -1,5 раза больше IQR. Кругами (°) обозначают отклонения. Внутри рамок выемки обозначают доверительный интервал, основанный на медиане ± 1,58 (IQR/sqrt n) (n=количество измерений). Кроме того, среднее значение обозначается черным квадратом, а символ креста (+) отображает стандартное отклонение. SPe-gCRYSTAL (n = 36), ILe-gCRYSTAL (n = 38), SPe-gCLASSIC (n = 35), ILe-gCLASSIC (n = 41), SPe-grCLASSIC + PRF (n = 38), ILNanobone (n = 42), ILBioOss (n = 34), SPControl (n = 30), and ILControl (n = 35).
Предположительно, эти различия объясняются тем, что могут быть существенно разные усилия, действующие на участки аугментации во временной шкале цикла регенерации костной ткани. В то время как в местах синус-лифтинга единственным повторяющимся усилием является дыхательная активность, создающая только линейные вертикальные перепады давления в среднем 15 мбар с многократными одиночными или множественными изменениями пикового давления в 1,5 бара при чихании [33] , субпериостальный участок аугментации в передней челюсти подвергается воздействию, возможно, гораздо более высоких и всенаправленных сил при разговоре, улыбке и приеме пищи. Это, возможно, приводит к микромодуляциям при взаимодействии BiSHB и MoSHB трансплантата и при взаимодействии BiSHB и MoSHB кости, которые превышают биологический порог [27-29] и приводят к снижению ангиогенеза [35].35]. Это вполне вероятное предположение может привести к наблюдаемой меньшей (био)механической стабильности аугментированной верхнечелюстной кости в передней челюсти, а также может объяснить, почему клинические испытания с использованием свободных гранулобиоматериалов (ксеногенных и синтетических различных марок), введенных в субпериостальные каркасы в передней челюсти по процедурам, описанным в литературе только для нижней челюсти [19-24], неудачны и с самого начала привели к простой волокнистой инкапсуляции, как и в случае с непервичными стабильно нагруженными зубными имплантатами [29], и требовали отмены. С другой стороны, после добавления в трансплантат MoSHB улучшенного насыщенного тромбоцитами фибрина (aPRF) (био)механическая стабильность переднего участка PeSPTT немного превосходит ITV, полученные в исследовании синус-лифтинга (рис. 18), и этим сильно подкрепляет доказательства, в которых PRF спровоцирует более быстрый и лучший ангиогенез и ослабление последствий микромодуляции хирургического участка PeSPTT выше биологического порога при реформации кости[36-39].
Таблица 1: Статистическая оценка проводилась с помощью одностороннего ANOVA-теста, параметрического t-критерия Стьюдента, по полученным результатам множественных сравнений по наименьшей значимой разнице критерия Фишера (LSD) для проверки средних значений момента вставки и дисперсии в каждой группе и средней значимости различий между всеми группами.
|
(a) |
||||||||||||||||
|
Средства сравнения |
||||||||||||||||
|
Сравнение для каждой пары с использованием параметрического t-критерия Стьюдента |
||||||||||||||||
|
Доверительный квантиль |
||||||||||||||||
|
t |
Альфа |
|||||||||||||||
|
1.97769 |
0.05 |
|||||||||||||||
|
(b) |
||||||||||||||||
|
LSD пороговая матрица Abs(Dif)-LSD |
||||||||||||||||
|
|
Easy-graft CRYSTAL_SP |
Easy-graft CLASSIC+PRF |
Easy-graft CLASSIC+PRF |
Контрольная Группа Нативная Кость Передняя-Клык_SP |
||||||||||||
|
Easy-graft CRYSTAL_SP |
-3.12 |
2.52 |
6.84 |
21.36 |
||||||||||||
|
Easy-graft CLASSIC + PRF_SP |
2.52 |
-3.04 |
1.28 |
15.79 |
||||||||||||
|
Easy-graft CLASSIC_SP |
6.84 |
1.28 |
-3.17 |
11.35 |
||||||||||||
|
Контрольная Группа Нативная Кость Передняя-Клык_SP |
21.36 |
15.79 |
11.35 |
-3.42 |
||||||||||||
|
Положительные значения показывают пары средних, которые существенно различаются. |
||||||||||||||||
|
(c) |
||||||||||||||||
|
Отчет |
||||||||||||||||
|
уровень |
Значение |
|||||||||||||||
|
Easy-graft CRYSTAL_SP |
A |
|
|
|
52.50 |
|||||||||||
|
Easy-graft CLASSIC + PRF_SP |
|
B |
|
|
46.89 |
|||||||||||
|
Easy-graft CLASSIC_SP |
|
|
C |
|
42.51 |
|||||||||||
|
Контрольная Группа Нативная Кость Передняя-Клык_SSP |
|
|
|
D |
27.87 |
|||||||||||
|
Уровни, не связанные одной буквой, статистически значимо различаются. |
||||||||||||||||
|
(d) |
||||||||||||||||
|
Отчет об упорядоченных расхождениях |
||||||||||||||||
|
Уровень |
по сравнению с |
Уровень |
Различие |
Стандартная ошибка оценки |
Нижний доверительный предел |
Верхний доверительный предел |
P значе-ние |
|||||||||
|
Easy-graft CRYSTAL_SP |
Контрольная Группа Нативная Кость Передняя-Клык_SP |
24.63 |
1.66 |
21.36 |
27.91 |
<0.0001 |
||||||||||
|
Easy-graft CLASSIC + PRF_SP |
Контрольная Группа Нативная Кость Передняя-Клык_SP |
19.03 |
1.64 |
15.79 |
22.27 |
<0.0001 |
||||||||||
|
Easy-graft CLASSIC_SP |
Контрольная Группа Нативная Кость Передняя-Клык_SP |
14.65 |
1.67 |
11.35 |
17.95 |
<0.0001 |
||||||||||
|
Easy-graft CRYSTAL_SP |
easy-graft CLASSIC_SP |
9.99 |
1.59 |
6.84 |
13.13 |
<0.0001 |
||||||||||
|
Easy-graft CRYSTAL_SP |
easy-graft CLASSIC + PRF_SP |
5.61 |
1.56 |
2.52 |
8.69 |
0.0005 |
||||||||||
|
Easy-graft CLASSIC + PRF_SP |
easy-graft CLASSIC_SP |
4.38 |
1.57 |
1.27 |
7.49 |
0.0060 |
||||||||||
Этот эксперимент [30, 31], клиническая картина [33] и кроме того, представленные исследования показывают, что биоматериалы, содержащие гидроксиапатит (HA), по-видимому, из-за более быстрого поглощения чистого bTCP обеспечивают более механически стабильное восстановление кости и нативной челюстной кости, что в клинической практике весьма приветствуется для последующего введения имплантата (рис.19). Этот факт может быть отнесен к очень медленному рассасыванию структурной плотности. Биохимическая природа HA, выступающая как структурное усиление окружающей восстановленной нативной кости, когда-то полностью остеоинтегрированной, сравнима с трубчатой архитектурой HA длинных костей млекопитающих (трубчатая архитектура HA длинных костей (остеон) представляет собой более высокую эволюционную стадию, чем сплетенные кости черепа и ребер). Для практикующего врача аддитивное использование трансплантатов BiSHB в сочетании с aPRF как для PeSPTT, так и для tHUCSL -INTRALIFT представляется предпочтительным для достижения максимально возможной биомеханической стабильности восстановленного альвеолярного гребня, и в настоящее время находится в стадии клинического исследования авторами в качестве расширения данного исследования.
|
Таблица 2: Статистическая оценка ITV, полученных в исследовании субпериостального туннельного метода (SP) и исследовании INTRALIFT (IL), проводилась с помощью одностороннего ANOVA-теста, параметрического t-критерия Стьюдента и по полученным результатам множественных сравнений по наименьшей значимой разнице критерия Фишера (LSD) для проверки средних значений момента вставки и дисперсии в каждой группе и средней значимости различий между всеми группами.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
5. Заключение
В соответствии с современными знаниям о структуре, биомеханике и физиологии регенерации костной ткани и интерпретируя результаты текущих и предшествующих клинических исследований [33], воспроизводимые высокие клинические показатели успеха в направленной регенерации костной ткани и имплантологии с наименьшей заболеваемостью пациентов зависят от нескольких решающих факторов в клинической практике с четкими клиническими рекомендациями и выводами в отношении знания биологии заживления, регенерации и восстановления костей.
5.1. Атравматическая и точная хирургия на
макроскопическом и микроскопическом уровне. Так как прерывание васкуляризации может привести к недостаточному
ангиогенезу в наиболее обширных участках аугментации, рассчитанных до
необходимых объемов костной ткани в 2 см3, которые находятся за пределами
«дефектов критических размеров» [34], следует травмировать как можно меньше кровеносных сосудов, избегая
полнослойных слизисто-надкостничных лоскутов в пользу субпериостальных
туннельных или карманных методов.
Пери- и эндостальные соединительные волокна Шарпея должны
быть чисто разрезаны, а не разорваны и разрезаны предпочтительно с помощью
ультразвуковых хирургических инструментов («Пьезотомов»), которые используют
кавитационный эффект для чистой надкостничной отслойки макроскопически (Рис. 3 и 4) и
микроскопически ( Рис. 1) [7], оставляя слой
камбия («колыбель остеобластов») непрерывным и полностью неповрежденным на
клеточном и функциональном уровне. В настоящее время широко рекомендуется
Пьезотомическая хирургия, чтобы в целом сохранить мягкие ткани и избежать
механических повреждений [49-51],
уменьшить ишемию тканей [52], и стимулировать
дифференцировку мезенхимальных стволовых клеток и заживление костей.
Последовательные результаты данного исследования в совокупности с результатами предыдущих аналогичных исследований [17, 33, 50, 51] по-видимому, подтверждают предположение о том, что использование Пьезотомической хирургии для подготовки участка аугментации может быть первым шагом к достижению постоянных высоких показателей успеха и не требует обширной подготовки хирурга по сравнению с традиционными сложными и технически трудновыполнимыми хирургическими методами.
5.2. Достаточная иммобилизация участка аугментации. Хирургически созданные субпериостальные и
эндостальные каркасы для увеличения костной массы должны восприниматься
практикующим врачом скорее как «места переломов», подобные «естественным»
переломам челюстных костей и их обязательной иммобилизации для правильного
заживления кости. Минимально инвазивные хирургические методы, такие как tHUCSL
- INTRALIFT [56] и Пьезотомически усиленный
субпериостальный туннель или карман (PeSPTT), не позволяют использовать
аутотрансплантированные, ксеногенные или синтетические твердые костные блоки,
поскольку они должны быть стабилизированы винтами остеосинтеза. Рыхлые
аутологичные, ксеногенные или синтетические гранулированные биоматериалы
склонны к макро- и микродвижениям под действием мышечных, дыхательных (в случае
верхнечелюстной пазухи) и/или усилий мягких тканей в нормальном
функционировании стоматогнатической и дыхательной систем, и, тем самым, могут
противодействовать надлежащей иммобилизации аугментационного каркаса, как
это предполагается результатами, представленными в предыдущем исследовании [33]. Таким образом, новый класс формуемых in situ и самозатвердевающих
биоматериалов, используемых в данном исследовании, представляется весьма
подходящим для минимально инвазивной направленной регенерации костной ткани для
достижения воспроизводимых положительных результатов и обеспечивает достаточный
(био)механический высокостабильный участок зубного имплантата достаточных
размеров. Этот класс биоматериалов, по-видимому, удовлетворяет биологическому
требованию надлежащей иммобилизации аугментационного каркаса для ненарушенной
естественной регенерации кости ниже предложенного порога микромобильности
100-150 м [29] в собственной костноблочной
микропористой консистенции и ее неподвижности на костной и периостальной
поверхности.
5.3. Использование биологически
активных аутологичных агентов, таких как насыщенная тромбоцитами плазма (PRP)
или улучшенный насыщенный тромбоцитами фибрин (aPRF). Можно считать
биологическим фактом, что все биосовместимые материалы (например, титан, ZiO,
PEEK, молочнокислые полимеры, биоглассы, bTCP, природный или синтетический
гидроксиапатит и т. д.) разрешены к остеоинтеграции, но сами по себе не
являются «остеоиндуктивными/проводящими». Отличия между различными видами
происхождения (человек, бык, лошадь, свинья, все происходящие из одного и того
же эволюционного ствола млекопитающих, водорослей, керамики, стекла, bTCP и HA)
и марками биоматериалов при экспериментальной микроскопической,
радиологической, клинической и статистической оценке результатов регенерации
костной ткани редко оказывают существенное влияние на работу практикующего
врача, поскольку клинические исследования как на животных, так и на людях почти
никогда не сообщают, был ли базальный слой камбия надкостницы интактным, и если
и как надкостница была прорезана для достижения безнапорного закрытия раны.
Хотя покрытие любого участка аугментации барьерными мембранами различного химического происхождения (PTFE, Титан, полимолочная кислота, коллаген и др.), по-прежнему предпочтительно в случаях предсуществующего и/или ятрогенного опустошения и разрушения надкостницы, его следует рассматривать как противопоказание, когда надкостница отделяется без повреждений от кости [57].
Лучшей альтернативой в обоих случаях может быть общая
замена барьерных мембран аутологичными мембранами aPRF, которые обеспечивают
доказанное физиологическое усиление ангиогенеза и роста костей [36-39], копируя и концентрируя активные биологические агенты через
центрифугирование, умножая эффект естественной конденсации фибрина на каждую
рану мягких и твердых тканей и биосовместимые имплантируемые материалы. В
отличие от производства PRP-концентратов подготовка aPRF легко интегрируется в своевременный поток операций GBR и не представляет
собой проблемы для хирурга, выполняющего операцию.
Результаты настоящего исследования подтверждают
экспериментальные данные о преимуществах более надежной регенерации костной
ткани при использовании aPRF и предполагают, что aPRF повышает биомеханическое
качество костной ткани до постоянного более высокого уровня в клинической
практике в сочетании с Пьезотомической хирургией и трансплантатами BiSHB,
чтобы, возможно, достичь лучших и более последовательных результатов при
меньшей заболеваемости пациентов по сравнению с традиционными методами.
5.4. Смена
парадигмы понимания управляемых процедур регенерации костной ткани в
клинической практике. Челюстно-лицевой хирургам предлагается отказаться от
(био)материально-технического взгляда на хирургические инструменты,
ориентированного на более общий взгляд на операции GBR, основанные на
биологических и физиологических фактах механизмов заживления костей. Как и в
диагностике и в хирургическом планировании, обычные практикующие врачи все
больше полагаются на готовые рецепты и программные хирургические
«вспомогательные средства», упуская из виду индивидуальную стоматогнатическую
динамику отдельного пациента. Хирургическое планирование и выполнение операции
должны строго следовать рекомендациям, данным биологией и динамикой
стоматогнатической системы, а не сборным «хирургическим шаблонам». Предложение
установить аутологичные костные трансплантаты как «золотой стандарт» в
стоматологической регенеративной терапии больше не может поддерживаться [58] и должно стать
философской дискуссией о том, должна ли регенерированная/дополненная кость быть
только нативной костью или явно механическим более резистивным соединением
нативной кости и синтетических биоматериалов («аргумент инородного тела») для
поддержания введенных сил другими « инородными телами», то есть зубными
имплантатами (сделанными из титана, ZiO, PEEK и т. д.).
Конфликт интересов
Авторы заявляют, что никакого конфликта интересов в связи с публикацией данной статьи не существует.
Список литературы
[1] G. H. Bourne, "The relative importance of periosteum and endosteum in bone healing and the relationship of vitamin C to their activities," Proceedings of the Royal Society of Medicine, vol. 37, no. 6, pp. 275-279,1944.
[2] D. Özçelik, T. Turan, F. Kabukcuoglu et al., "Bone induction capacity of the periosteum and neonatal dura in the setting of the rat zygomatic arch fracture model," Archives of Facial Plastic Surgery, vol. 5, no. 4, pp. 301-308, 2003.
[3] t Ortak, R. Özdemir, A. Uysal et al., "Osteogenic capacities of periost grafts, periost flaps and prefabricated periosteal flaps: experimental study," Journal of Craniofacial Surgery, vol. 16, no. 4, pp. 594-600, 2005.
[4] C. A. Squier, S. Ghoneim, and C. R. Kremenak, "Ultrastructure of the periosteum from membrane bone," Journal of Anatomy, vol. 171, pp. 233-239,1990.
[5] S. Srouji, T. Kizhner, D. Ben David, M. Riminucci, P. Bianco, and E. Livne, "The schneiderian membrane contains osteopro- genitor cells: in vivo and in vitro study," Calcified Tissue International, vol. 84, no. 2, pp. 138-145, 2009.
[6] A. Troedhan, A. Kurrek, and M. Wainwright, "Biological principles and physiology of bone regeneration under the schnei- derian membrane after sinus lift surgery: a radiological study in 14 patients treated with the transcrestal hydrodynamic ultrasonic cavitational sinus lift (Intralift)," International Journal of Dentistry, vol. 2012, Article ID 576238, 12 pages, 2012.
[7] A. Troedhan, A. Kurrek, M. Wainwright, and S. Jank, "Schneiderian membrane detachment using transcrestal Hydrodynamic Ultrasonic Cavitational Sinus Lift: a human cadaver head study and histologic analysis," Journal of Oral and Maxillofacial Surgery, vol. 72, no. 8, pp. 1503.e1-1503.e10, 2014.
[8] P. J. Boyne, L. C. Lilly, R. E. Marx et al., "De novo bone induction by recombinant human bone morphogenetic protein-2 (rhBMP-2) in maxillary sinus floor augmentation," Journal of Oral and Maxillofacial Surgery, vol. 63, no. 12, pp. 1693-1707, 2005.
[9] D. G. Smiler and R. E. Holmes, "Sinus lift procedure using porous hydroxyapatite: a preliminary clinical report," The Journal of Oral Implantology, vol. 13, no. 2, pp. 239-253, 1986.
[10] M. S. Block and J. N. Kent, "Sinus augmentation for dental implants: the use of autogenous bone," Journal of Oral and Maxillofacial Surgery, vol. 55, no. 11, pp. 1281-1286, 1997.
[11] G. Cordioli, C. Mazzocco, E. Schepers, E. Brugnolo, and Z. Majzoub, "Maxillary sinus floor augmentation using bioactive glass granules and autogenous bone with simultaneous implant placement," Clinical Oral Implants Research, vol. 12, no. 3, pp. 270-278, 2001.
[12] G. V. Cammack II, M. Nevins, D. S. Clem III, J. P. Hatch, and J. T. Mellonig, "Histologic evaluation of mineralized and demineralized freeze-dried bone allograft for ridge and sinus augmentations," International Journal of Periodontics and Restorative Dentistry, vol. 25, no. 3, pp. 231-237, 2005.
[13] S. A. Zijderveld, I. R. Zerbo, J. P. van den Bergh, E. A. Schulten, and C. M. ten Bruggenkate, "Maxillary sinus floor augmentation using a beta-tricalcium phosphate (Cerasorb) alone compared to autogenous bone grafts," The International Journal of Oral & Maxillofacial Implants, vol. 20, no. 3, pp. 432-440, 2005.
[14] G. Szabó, L. Huys, P. Coulthard et al., "A prospective multi- center randomized clinical trial of autogenous bone versus tricalcium phosphate graft alone for bilateral sinus elevation: histologic and histomorphometric evaluation," International Journal of Oral & Maxillofacial Implants, vol. 20, no. 3, pp. 371-381, 2005.
[15] S. S. Wallace and S. J. Froum, "Effect of maxillary sinus augmentation on the survival of endosseous dental implants. A systematic review," Annals of Periodontology, vol. 8, no. 1, pp. 328-343, 2003.
[16] F. Stelzle and K.-U. Benner, "Evaluation of different methods of indirect sinus floor elevation for elevation heights of 10 mm: an experimental ex vivo study," Clinical Implant Dentistry and Related Research, vol. 13, no. 2, pp. 124-133, 2011.
[17] A. Troedhan, A. Kurrek, M. Wainwright, I. Schlichting, B. Fischak-Treitl, and M. Ladentrog, "The transcrestal hydrodynamic ultrasonic cavitational sinuslift: results of a 2-year prospective multicentre study on 404 patients, 446 sinuslift sites and 637 inserted implants," Open Journal of Stomatology, vol. 3, no. 9, pp. 471-485, 2013.
[18] S. S. Huja, S. A. Fernandez, K. J. Hill, and Y. Li, "Remodeling dynamics in the alveolar process in skeletally mature dogs," The Anatomical Record Part A: Discoveries in Molecular, Cellular, and Evolutionary Biology, vol. 288, no. 12, pp. 1243-1249, 2006.
[19] (j) N. Kent, J. H. Quinn, M. F. Zide, I. M. Finger, M. Jarcho, and S. S. Rothstein, "Correction of alveolar ridge deficiencies with nonresorbable hydroxylapatite," The Journal of the American Dental Association, vol. 105, no. 6, pp. 993-1001,1982.
[20] S. S. Rothstein, D. A. Paris, and M. P. Zacek, "Use of hydroxylapatite for the augmentation of deficient alveolar ridges," Journal of Oral and Maxillofacial Surgery, vol. 42, no. 4, pp. 224-230, 1984.
[21] R. H. Propper, "A technique for controlled placement of hydroxylapatite over atrophic mandibular ridges," Journal ofOral and Maxillofacial Surgery, vol. 43, no. 6, pp. 469-470, 1985.
[22] F. Härle and T. Kreusch, "Augmentation of the alveolar ridges with hydroxylapatite in a Vicryl tube," International Journal of Oral and Maxillofacial Surgery, vol. 20, no. 3, pp. 144-148, 1991.
[23] Y. Kurihara, T. Wakatsuki, Y. Harada et al., "Mandibular alveolar ridge extension method using a surgical splint with porous hydroxyapatite (HAP) particles," The Bulletin of Tokyo Dental College, vol. 32, no. 2, pp. 71-79,1991.
[24] M. L. Nevins, M. Camelo, P. Schupbach, B. Friedland, J. M. B. Camelo, and D. M. Kim, "Minimally invasive alveolar ridge augmentation procedure (tunneling technique) using rhPDGF- BB in combination with three matrices: a case series," The International Journal of Periodontics & Restorative Dentistry, vol. 29, no. 4, pp. 371-383, 2009.
[25] M. Nevins, D. Garber, J. J. Hanratty et al., "Human histologic evaluation of anorganic bovine bone mineral combined with recombinant human platelet-derived growth factor BB in maxillary sinus augmentation: case series study," The International Journal of Periodontics & Restorative Dentistry, vol. 29, no. 6, pp. 583-591, 2009.
[26] E. Martinez-Sanz, O. P. Varghese, M. Kisiel et al., "Minimally invasive mandibular bone augmentation using injectable hydrogels," Journal of Tissue Engineering and Regenerative Medicine, vol. 6, no. 3, pp. s15-s23, 2012.
[27] P. Aspenberg, S. Goodman, S. Toksvig-Larsen, L. Ryd, and T. Albrektsson, "Intermittent micromotion inhibits bone ingrowth. Titanium implants in rabbits," Acta Orthopaedica Scandinavica, vol. 63, no. 2, pp. 141-145, 1992.
[28] M. Jasty, C. Bragdon, D. Burke, D. O'Connor, J. Lowenstein, and W. H. Harris, "In vivo skeletal responses to porous-surfaced implants subjected to small induced motions," The Journal of Bone and Joint Surgery—American Volume, vol. 79, no. 5, pp. 707-714,1997.
[29] S.-S. Gao, Y.-R. Zhang, Z.-L. Zhu, and H.-Y. Yu, "Micromotions and combined damages at the dental implant/bone interface," International Journal of Oral Science, vol. 4, no. 4, pp. 182-188, 2012.
[30] P. R. Schmidlin, F. Nicholls, A. Kruse, R. A. Zwahlen, and F. E. Weber, "Evaluation of moldable, in situ hardening calcium phosphate bone graft substitutes," Clinical Oral Implants Research, vol. 24, no. 2, pp. 149-157, 2013.
[31] I. Binderman, A. Yaffe, Y. Samuni, H. Bahar, J. Choukroun, and P. Russe, "Tissue engineering of bone: critical evaluation of scaffold selection," in Bone Regeneration, InTech, 2012.
[32] (h) M. Frost, "A 2003 update of bone physiology and Wolff's law for clinicians," The Angle Orthodontist, vol. 74, no. 1, pp. 3-15, 2004.
[1] A. Troedhan, I. Schlichting, A. Kurrek, and M. Wainwright, "Primary implant stability in augmented sinuslift-sites after completed bone regeneration: a randomized controlled clinical study comparing four subantrally inserted biomaterials," Scientific Reports, vol. 4, article 5877, 2014.
[2] A. Udagawa, S. Sato, A. Hasuike, M. Kishida, Y. Arai, and K. Ito, "Micro-CT observation of angiogenesis in bone regeneration," Clinical Oral Implants Research, vol. 24, no. 7, pp. 787-792,2013.
[3] A. Mammoto, K. M. Connor, T. Mammoto et al., "A mechano- sensitive transcriptional mechanism that controls angiogene- sis," Nature, vol. 457, no. 7233, pp. 1103-1108, 2009.
[4] t Mammoto, A. Jiang, E. Jiang, and A. Mammoto, "Platelet rich plasma extract promotes angiogenesis through the angiopoietin1-Tie2 pathway," Microvascular Research, vol. 89, pp. 15-24, 2013.
[5] A. Ballini, M. Scivetti, S. Cantore, B. Rapone, G. Favia, and R. Grassi, "Tissuue engineering in maxillar sinus lifting: a comparation of differents grafts and confocal laser scanning microscopic evaluation," in Bone Regeneration, H. Tal, Ed., chapter 5, InTech, Rijeka, Croatia, 2012.
[6] C. L. M. Bao, E. Y. Teo, M. S. Chong, Y. Liu, M. Choolani, and J. K. Chan, "Advances in bone tissue engineering," in Regenerative Medicine and Tissue Engineering, pp. 599-6144, InTech, Rijeka, Croatia, 2013.
[7] N. Lohse, J. Schulz, and H. Schliephake, "Effect of fibrin on osteogenic differentiation and VEGF expression of bone marrow stromal cells in mineralised scaffolds: a three-dimensional analysis," European Cells & Materials, vol. 23, pp. 413-424, 2012.
[8] Z. Wang, Y. Weng, S. Lu et al., "Osteoblastic mesenchymal stem cell sheet combined with Choukroun platelet-rich fibrin induces bone formation at an ectopic site," Journal of Biomedical Materials Research PartB: Applied Biomaterials, 2014.
[9] I. Turkyilmaz and E. A. McGlumphy, "Influence of bone density on implant stability parameters and implant success: a retrospective clinical study," BMC Oral Health, vol. 8, no. 1, article 32, 2008.
[10] P. Trisi, G. Perfetti, E. Baldoni, D. Berardi, M. Colagiovanni, and G. Scogna, "Implant micromotion is related to peak insertion torque and bone density," Clinical Oral Implants Research, vol. 20, no. 5, pp. 467-471, 2009.
[11] L. R. Walker, G. A. Morris, and P. J. Novotny, "Implant inser- tional torque values predict outcomes," Journal of Oral and Maxillofacial Surgery, vol. 69, no. 5, pp. 1344-1349, 2011.
[12] G. Augustin, A. Antabak, and S. Davila, "The periosteum. Part 1: anatomy, histology and molecular biology," Injury, vol. 38, no. 10, pp. 1115-1130, 2007.
[13] (j) E. Aaron, "Periosteal sharpey's fibers: a novel bone matrix regulatory system," Frontiers in Endocrinology, vol. 3, article 98, 2012.
[14] A. C. Vailas, D. M. Deluna, L. L. Lewis, S. L. Curwin, R. R. Roy, and E. K. Alford, "Adaptation of bone and tendon to prolonged hindlimb suspension in rats," Journal of Applied Physiology, vol. 65, no. 1, pp. 373-376, 1988.
[15] t J. Wronski and E. R. Morey, "Effect of spaceflight on periosteal bone formation in rats," The American Journal of Physiology— Regulatory Integrative and Comparative Physiology, vol. 244, no. 3, pp. R305-R309, 1983.
[16] t Matsuura, K. Tokutomi, M. Sasaki, M. Katafuchi, E. Mizu- machi, and H. Sato, "Distinct characteristics of mandibular bone collagen relative to long bone collagen: relevance to clinical dentistry," BioMed Research International, vol. 2014, Article ID 769414, 9 pages, 2014.
[17] A. Troedhan, A. Kurrek, and M. Wainwright, "Ultrasonic piezotome surgery: is it a benefit for our patients and does it extend surgery time? A retrospective comparative study on the removal of 100 impacted mandibular 3rd molars," Open Journal of Stomatology, vol. 1, no. 4, pp. 179-184, 2011.
[18] M. Goyal, K. Marya, A. Jhamb et al., "Comparative evaluation of surgical outcome after removal of impacted mandibular third molars using a Piezotome or a conventional handpiece: a prospective study," British Journal of Oral and Maxillofacial Surgery, vol. 50, no. 6, pp. 556-561, 2012.
[19] S. Pappalardo and R. Guarnieri, "Randomized clinical study comparing piezosurgery and conventional rotatory surgery in mandibular cyst enucleation," Journal of Cranio-Maxillofacial Surgery, vol. 42, no. 5, pp. e80-e85, 2013.
[20] V. N. Suchkova, R. B. Baggs, S. K. Sahni, and C. W. Francis, "Ultrasound improves tissue perfusion in ischemic tissue through a nitric oxide dependent mechanism," Thrombosis and Haemostasis, vol. 88, no. 5, pp. 865-870, 2002.
[21] N. Doan, P. Reher, S. Meghji, and M. Harris, "In vitro effects of therapeutic ultrasound on cell proliferation, protein synthesis, and cytokine production by human fibroblasts, osteoblasts, and monocytes," Journal of Oral and Maxillofacial Surgery, vol. 57, no. 4, pp. 409-420, 1999.
[22] S. Mouraret, K. S. Houschyar, D. J. Hunter et al., "Cell viability after osteotomy and bone harvesting: comparison of piezoelectric surgery and conventional bur," International Journal of Oral & Maxillofacial Surgery, vol. 43, no. 8, pp. 966-971, 2014.
[23] (j) Reside, E. Everett, R. Padilla et al., "In vivo assessment of bone healing following piezotome ultrasonic instrumentation," Clinical Implant Dentistry and Related Research, 2013.
[24] A. C. Troedhan, A. Kurrek, M. Wainwright, and S. Jank, "Hydro- dynamic ultrasonic sinus floor elevation—an experimental study in sheep," Journal of Oral and Maxillofacial Surgery, vol. 68, no. 5, pp. 1125-1130, 2010.
[25] E. A. J. M. Schulten, H.-J. Prins, J. R. Overman, M. N. Helder, C. M. ten Bruggenkate, and J. Klein-Nulend, "A novel approach revealing the effect of a collagenous membrane on osteoconduction in maxillary sinus floor elevation with tricalcium phosphate," European Cells and Materials, vol. 25, pp. 215-228, 2012.
M. del Fabbro, G. Rosano, and S. Taschieri, "Implant survival rates after maxillary sinus augmentation," European Journal of Oral Sciences, vol. 116, no. 6, pp. 497-506, 2008


 Google Play
Google Play App Store
App Store